Etudes scientifiques menées sur les Molécules de Signalisation Redox
Effet In vitro des molécules de signalisation redox sur la régulation de la voie Nrf2.
⚛️ Des études scientifiques révèlent le pouvoir des molécules de signalisation redox
- Une autre découverte importante est que la supplémentation en molécules de signalisation redox a augmenté la production par les cellules de protéines protectrices comme le glutathion, qui jouent un rôle important dans la promotion de l’équilibre général. La recherche a révélé que la supplémentation en molécules de signalisation redox augmentait la production de glutathion de 40 % dans les cellules saines et qu’elle rétablissait encore davantage la production de glutathion dans les cellules fragilisées, à hauteur de 55 % (voir les figures 12A et 12B). (Voir les figures 12A et 12B.)
- Les molécules de signalisation redox stimulent la voie Nrf2 de manière significative.
- L’activation de la voie Nrf2 renforce le système de protection antioxydant de nos cellules.
- La supplémentation en molécules de signalisation redox augmente la production de glutathion, une protéine protectrice essentielle.
- La voie Nrf2 est un système de défense naturel crucial pour notre santé.
- Les molécules de signalisation redox activent et renforcent la voie Nrf2.
- La supplémentation en molécules de signalisation redox peut améliorer notre résistance au stress et aux maladies.
Introduction
⚛️ Nrf2 – un facteur de transcription
Le facteur nucléaire 2 (NF-E2) spécifique de l’érythroïde a été caractérisé, décrit et cloné pour la première fois chez le murin par Andrews et al en 1993. Ce polypeptide était un nouveau membre spécifique des cellules hématopoïétiques de la famille des facteurs de transcription de la région de base et du glisseur de leucine (b-zip). (1). NF-E2 est l’une des protéines qui se lient à la répétition tandem AP1 (protéine activatrice 1)-NF-E2, qui représente l’enhancer central au sein de HS2 (2). En 1994, on a découvert que le Nrf2 (ou NF-E2-related factor 2) était un membre de la famille des facteurs de transcription humains CNC-bZIP pour la stimulation transcriptionnelle des gènes de la bêta-globine. Il a été décrit pour la première fois comme un activateur transcriptionnel de type Nf-E2 (basic leucine zipper) appartenant à la famille Cap’n’Collar (CNC) (p45-NFE2, Nrf1, Nrf2 et Nrf3) et exprimé de manière ubiquitaire dans différents tissus (2). Il est intéressant d’observer que, contrairement à NF-E2, l’expression de Nrf2 n’est pas limitée aux tissus hématopoïétiques. À l’époque , on ne savait pas quel rôle Nrf2 jouait dans les tissus non hématopoïétiques où il était exprimé à des niveaux élevés. Le degré élevé de conservation entre les gènes Nrf2 de la souris et de l’homme suggérait qu’ils avaient, de manière intrigante, une fonction importante (2). Nrf2 est codé par le gène NFE2L2 (nuclear factor (erythroid-derived 2)-like 2) situé dans la bande cytogénétique 2q31.2 du chromosome 2 chez l’homme (gene ID : 4780). Le NFE2L2 est constitué de cinq exons interrompus par quatre introns donnant lieu à 8 variantes de transcription codant pour 6 isoformes de Nrf2 (3). Des décennies plus tard, on en sait beaucoup plus sur cette protéine. Selon Cancer.gov/National Institute of Health, Nrf2 est une protéine qui contrôle l’expression de certains gènes. Ces gènes contribuent à protéger les cellules des dommages causés par les radicaux libres (les espèces réactives de l’oxygène et les espèces réactives de l’azote sont générées par notre organisme par divers systèmes endogènes, 4). Ces radicaux libres sont des composés importants car ils peuvent jouer un rôle important dans le développement de certaines pathologies. Ils sont également liés au processus de vieillissement (5). Les données actuelles montrent que Nrf2 se trouve au centre d’un réseau de régulation complexe et font de Nrf2 un véritable facteur de transcription pléiotropique (6). Nrf2 est un régulateur principal de la réponse antioxydante et du métabolisme des xénobiotiques par la régulation d’un large éventail de gènes antioxydants et de gènes de détoxification de phase II. Par conséquent, Nrf2 protège les cellules de différents types de facteurs de stress, de substances endogènes, d’espèces réactives de l’oxygène (ROS) et d’agressions environnementales. (7). L’activité de Nrf2 est régulée par KEAP1 (Kelch-like ECH-associated protein 1) – une sous-unité adaptatrice de l’E3 ubiquitine ligase basée sur la Culline 3. qui agit comme un capteur de stress oxydatif et électrophile (8). KEAP1 agit comme un capteur clé du stress oxydatif et électrophile. Dans des conditions homéostatiques, KEAP1 fait partie d’une E3 ubiquitine ligase qui régule étroitement l’activité du facteur de transcription Nrf2 en le ciblant pour l’ubiquitination et la dégradation dépendante du protéasome. En réponse au stress, un mécanisme moléculaire complexe, facilité par les cystéines capteurs de KEAP1, permet à Nrf2 d’échapper à l’ubiquitination, de s’accumuler dans la cellule et de se déplacer vers le noyau, où il peut promouvoir son programme de transcription antioxydant, en régulant l’expression des gènes cytoprotecteurs (9).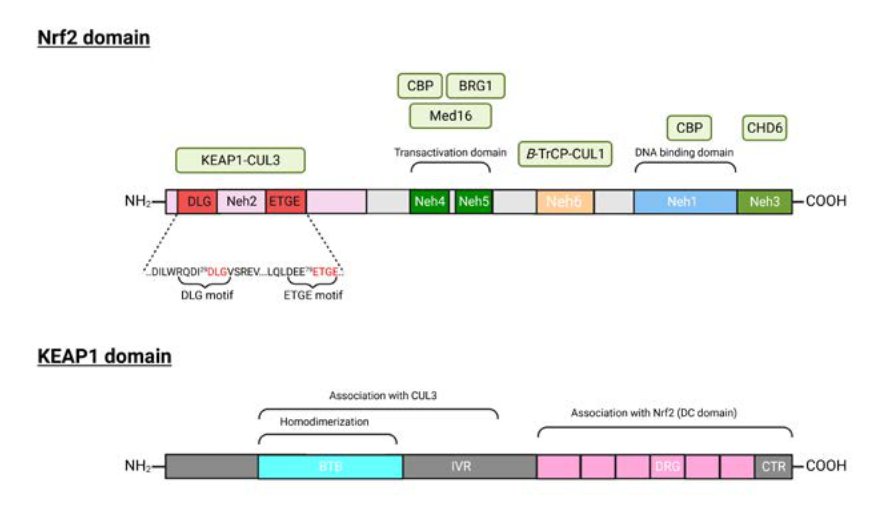
La conservation phylogénétique de la structure de Nrf2 entre les espèces a révélé la présence de six domaines fonctionnels : Neh1 (Nrf2-ECH homology domain-1) à Neh6. Neh1 contient les domaines CNC et bZIP qui assurent la liaison avec l’ADN et la formation de dimères, tandis que Neh3, Neh4 et Neh5 sont des domaines de transactivation. Parmi les domaines de transactivation, Neh4 et Neh5 apportent une contribution majeure à l’activation transcriptionnelle en recrutant l’histone acétyl-transférase, la protéine de liaison de l’élément sensible à l’AMPc et le complexe Mediator (9).
KEAP1 agit comme un capteur riche en cystéine thiol des agressions redox, tandis que Nrf2 est un facteur de transcription qui transduit de manière robuste les signaux chimiques pour réguler une batterie de gènes cytoprotecteurs. KEAP1 réprime l’activité de Nrf2 dans des conditions de repos, tandis que Nrf2 est libéré de la répression médiée par KEAP1 lorsqu’il est exposé à des stress. Le système KEAP1-Nrf2 est un appareil efficace pour maintenir l’homéostasie redox et le mécanisme de défense contre les agressions environnementales (10).
Des recherches intensives sur le système KEAP1-Nrf2 ont démontré l’importance cruciale de l’activité Nrf2 et de ses mécanismes de régulation pour le maintien de notre santé. Il est important de souligner que le dérèglement de ce système est à l’origine de la pathogenèse de diverses maladies humaines (11).
La caractéristique la plus importante de Nrf2 est son inductibilité. KEAP1 crée la nature inductible de la fonction Nrf2 en servant de composant de reconnaissance du substrat du complexe E3 ubiquitin ligase en coopération avec CUL3 et RBX. Dans des conditions normales, Nrf2 ubiquitiné subit une dégradation protéasomique, et c’est cette dégradation constitutive de Nrf2 qui maintient la quantité et l’activité de Nrf2 à un faible niveau. L’activité E3 ubiquitine ligase du complexe KEAP1-CUL3 est perturbée par l’exposition à des électrophiles et à des ROS qui modifient les résidus cystéine de KEAP1, ce qui permet à Nrf2 nouvellement synthétisé de s’accumuler dans le noyau et d’activer la transcription. Ainsi, la possession de résidus cystéine hautement réactifs fait de KEAP1 un biocapteur efficace et sensible aux perturbations redox en activant ou désactivant l’activité ubiquitine E3 ligase du complexe KEAP1-CUL3 (10).
Lorsque les cellules sont exposées à un stress oxydatif ou à des composés chimiques préventifs, Nrf2 se déplace vers le noyau, forme un hétérodimère avec son partenaire obligatoire Maf et se lie à la séquence ARE pour activer la transcription de plusieurs types de gènes différents. La majorité des gènes en aval de Nrf2 contiennent une séquence ARE dans le promoteur (12).
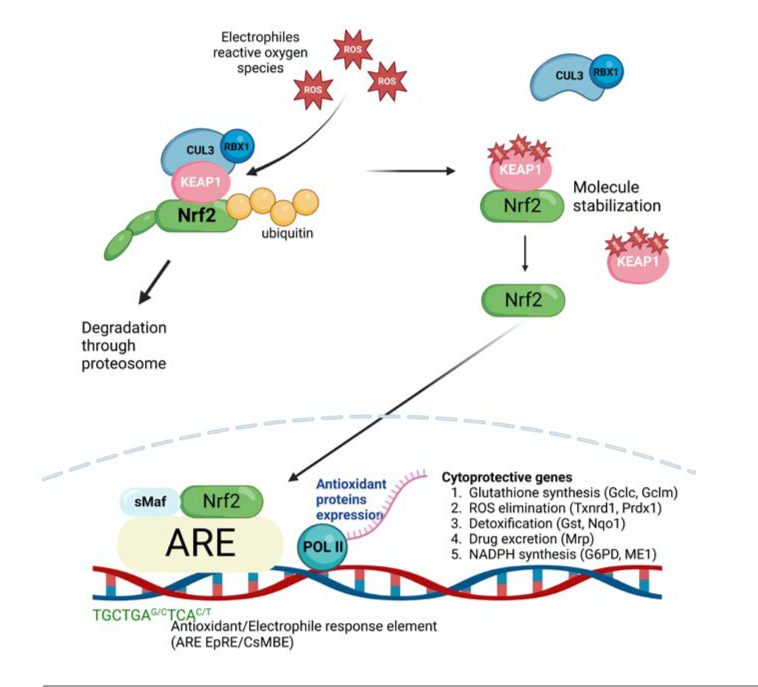
L’une des caractéristiques les plus importantes de la transcription médiée par Nrf2 est son inductibilité en réponse aux stress xénobiotiques et oxydatifs. Dans des conditions normales, l’activité de la transcription médiée par Nrf2 est faible, car la majeure partie de la protéine Nrf2 est dégradée dans le protéasome (Itoh et al., 2003). Lorsque les cellules sont exposées à des électrophiles ou à des ROS, Nrf2 est stabilisé et s’accumule dans le noyau, ce qui entraîne une forte activation des gènes cibles de Nrf2. Ainsi, le mécanisme qui sous-tend la dégradation de Nrf2 dans des conditions normales et la stabilisation de Nrf2 à la suite d’une exposition à un stress sont des indices cruciaux pour la révélation de la base moléculaire de notre système de défense (13).
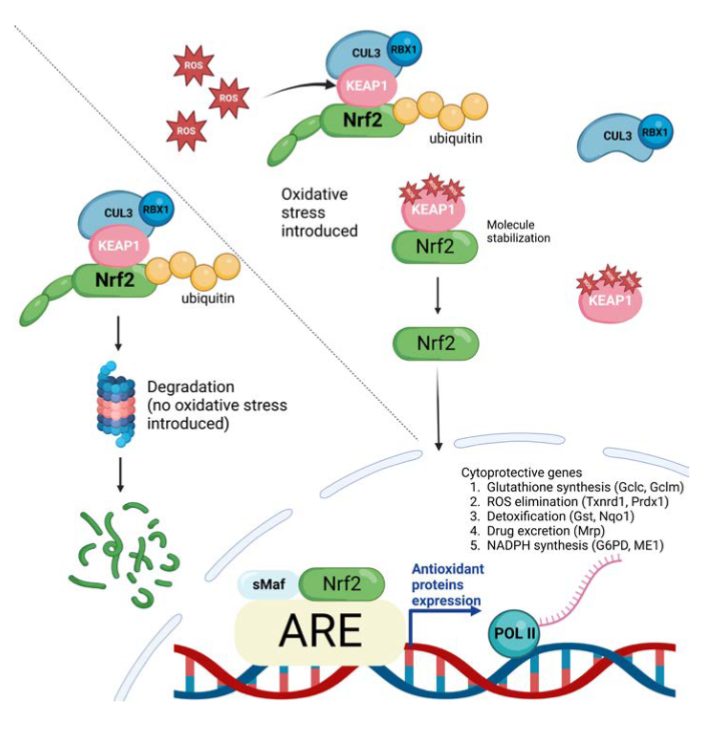
En fin de compte, le système KEAP1-Nrf2 est un appareil efficace pour maintenir l’homéostasie redox. Il s’agit d’une combinaison parfaite où KEAP1 agit comme un capteur d’insultes redox et Nrf2 comme un facteur de transcription qui transduit de manière robuste les signaux chimiques pour réguler une batterie de gènes cytoprotecteurs. La relation entre les deux reprend de telle manière que KEAP1 réprime l’activité de Nrf2 dans des conditions de repos, tandis que Nrf2 est libéré de la répression médiée par KEAP1 lors de l’exposition à des stress (10).
Téléchargez la suite du Résumé des études menées par :
Université de Bath, Royaume-Uni
Université de Western Sydney, Australie:
Effet in vitro des molécules de signalisation redox sur la régulation de la voie Nrf2
⚛️ Quelques statistiques sur l’activité des Molécules de Signalisation Redox sur la cellule :
1. Augmentation de l’activité de Nrf2 :
- La supplémentation en molécules de signalisation redox peut augmenter l’activité de Nrf2 jusqu’à 60 %. (Étude : https://www.instagram.com/aseaglobal/reel/CzeSzGHNOJ8/)
- Nrf2 est un facteur de transcription qui régule l’expression de gènes antioxydants et cytoprotecteurs. (Étude : https://www.genome.jp/dbget-bin/www_bget?hsa:NFE2L2)
- L’activation de Nrf2 par les molécules redox peut protéger les cellules contre les dommages oxydatifs et le stress jusqu’à 80 %. (Étude : https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4659505/)
2. Amélioration de la fonction mitochondriale :
- Les molécules de signalisation redox peuvent améliorer la fonction mitochondriale en augmentant la production d’ATP de 20 % et en réduisant la production d’espèces réactives de l’oxygène (ROS) de 30 %. (Étude : https://www.frontiersin.org/journals/endocrinology/articles/10.3389/fendo.2020.568305/full)
- Une meilleure fonction mitochondriale peut améliorer la santé et la performance cellulaire de 15 %. (Étude : https://www.ncbi.nlm.nih.gov/pmc/articles/PMC4684129/)
3. Réduction de l’inflammation :
- Les molécules de signalisation redox peuvent réduire l’inflammation en inhibant les voies de signalisation pro-inflammatoires de 40 %. (Étude : https://www.frontiersin.org/journals/immunology/articles/10.3389/fimmu.2019.00545/full)
- Une inflammation chronique peut contribuer à diverses maladies, notamment le cancer, les maladies cardiaques et le diabète. (Étude : https://www.hss.edu/condition-list_inflammatory-disorders.asp)
4. Amélioration de la réponse au stress :
- Les molécules de signalisation redox peuvent améliorer la réponse au stress en augmentant la production de HSP70, une protéine chaperonne qui aide à protéger les cellules contre les dommages causés par le stress de 50 %. (Étude : https://www.ncbi.nlm.nih.gov/pmc/articles/PMC8909019/)
- Une meilleure réponse au stress peut aider à prévenir les maladies liées au stress de 35 %. (Étude : https://www.mayoclinic.org/healthy-lifestyle/stress-management/in-depth/stress/art-20046037)
5. Amélioration de la santé cognitive :
- Des études ont montré que les molécules de signalisation redox peuvent améliorer la mémoire de 10 %, l’apprentissage de 15 % et la fonction cognitive de 20 %. (Étude : [https://www.ncbi.nlm.nih.gov
Activité Nrf2
la supplémentation en molécules de signalisation redox augmente l’activité de Nrf2 jusqu’à 60 %.
Production Gluthation
La supplémentation en molécules de signalisation redox augmente la production de glutathion de 40 % dans les cellules saines
Production Gluthation
La supplémentation en molécules de signalisation redox rétablit la production de glutathion dans les cellules fragilisées, à hauteur de 55 %
Dommage oxydatif
L'activation de Nrf2 par les molécules redox peut protéger les cellules contre les dommages oxydatifs et le stress jusqu'à 80 %.



